Chuyên mục
| Đang trực tuyến : | 6467 |
| Tổng truy cập : | 57,998 |
Khoa học - Y dược
Triển vọng mới trong sản xuất thuốc điều trị nhiễm trùng ruột (07/04/2016)
Nhiễm khuẩn Clostridium difficile trong các bệnh viện và các cơ sở chăm sóc y tế đang trở thành một vấn đề y tế cấp bách. Vi khuẩn này có khả năng tiết ra các độc tố tiêu diệt các tế bào trong ruột gây tiêu chảy và viêm đại tràng đe dọa sự sống của bệnh nhân. Việc sử dụng chất ức chế tự nhiên các độc tố này, có tên là InsP6, đã được thử nghiệm trong các ống thí nghiệm, không mang lại hiệu quả khi dùng đường uống. Các phương pháp truyền thống nhằm tối ưu hóa InsP6 cho đến nay vẫn chưa thành công.
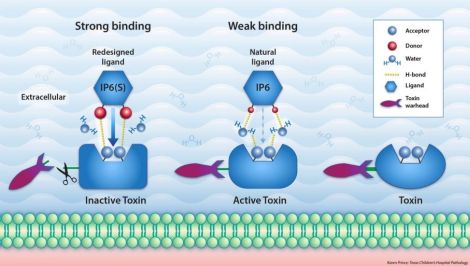
InsP6, chất ức chế tự nhiên hoặc phối tử độc tố của vi khuẩn Clostridium difficile liên kết yếu ớt với độc tố. Điều này dẫn đến các độc tố còn lại vẫn hoạt động (hình giữa). Việc biến đổi một nguyên tử đơn trong InsP6 thành dạng InsP6 (S) làm cho liên kết với các độc tố mạnh hơn và bất hoạt của chất đó (hình bên trái). Nguồn: T. Savidge (BCM); K. Prince (TCH).
Tuy nhiên, mới đây các nhà nghiên cứu tại Trường Đại học Y khoa Baylor đã nhận thấy việc biến đổi một nguyên tử trong InsP6 có thể gia tăng khả năng trung hòa chất độc của nó khoảng 26 lần. Kết quả của công trình nghiên cứu này đã được đăng trên tạp chí Science Advances.
“Độc tố, có tên gọi là TcdA và TcdB, là các phân tử rất lớn có khả năng giết chết các tế bào hiệu quả. Nó giống như một đầu đạn hạt nhân được phóng vào các tế bào để giết chết các tế bào. Các độc tố này có thể liên kết với tế bào và các tế bào tiếp nhận chúng vào bên trong một các túi màng tế bào có tên là nội bào (endosome). Không phải tất cả các độc tố sẽ thoát ra ngoài cái túi này để tiêu diệt các tế bào, mà chỉ các “đầu đạn” nhỏ xíu thò ra. Bộ phận khác của độc tố sẽ cảm nhận thấy khi đầu đạn ra thò ngoài túi và phân giải nó. Đầu đạn phóng ra sẽ gây trở ngại cho các chức năng cơ bản của tế bào và giết chết tế bào”, Tiến sỹ Tor Savidge, Phó giáo sư Bệnh lý học và Miễn dịch Khoa nhi, Giám đốc Phòng thí nghiệm Savidge thuộc Trung tâm Microbiome Children Texas, Tác giả chính của bài báo, cho biết.
Để trung hòa các chất độc này, các nhà khoa học “nhắm đích” phần giác quan khi các đầu đạn vẫn nằm bên trong tế bào, có tên là chất điều chế thể lập dị (allosteric modulator). Khi các đầu đạn phóng ra bên ngoài tế bào, nó sẽ bị trung hòa.
Thông qua phân tích và thử nghiệm hàng nửa triệu phân tử trong cơ sở dữ liệu lớn. Các nhà khoa học dò tìm các phân tử có khả năng liên kết với chất điều chế di lập thể và kích hoạt các đầu đạn phóng sớm. Tiến sỹ Numan Oezguen, thành viên phòng thí nghiệm của Savidge, đã dùng thuốc “ảo” sàng lọc để xác định các phân tử có khả năng liên kết với chất điều chế dị lập thể. Một trong những chiến lược sàng lọc của ông bao gồm việc tạo ra các cấu trúc ảo 3-D của các phân tử, phóng chúng trên một màn hình lớn và sử dụng các loại kính 3-D để xác định các tương tác có khả năng xảy ra giữa các phân tử. Các phân tử được phân tích có khả năng liên kết với chất điều chế di lập thể sẽ được đưa vào thử nghiệm trong phòng thí nghiệm.
“Chúng tôi phát hiện thấy cơ chế dị lập thể rất phức tạp. Bạn có thể tìm thấy cái gì đó mà bạn nghĩ có khả năng liên kết tốt, và bạn cho rằng nó sẽ là ứng cử viên sáng giá, tuy nhiên, nó không phải như vậy. Nó liên kết tốt, nhưng nó lại không kích hoạt giải phóng sớm các đầu đạn”, Savidge cho biết.
Kết quả này thúc đẩy các nhà nghiên cứu hiểu rõ hơn điều gì làm cho sự tương tác giữa các phân tử mạnh hơn hoặc yếu hơn. Phân tích tổng hợp của họ về nhiều phân tử đã mang lại sự hiểu biết sâu sắc cách thức nước góp phần vào các tương tác phân tử, đặc biệt là sự tham gia của các liên kết hyđrô, một trong những liên kết quan trọng nhất giữa các phân tử. Vai trò của liên kết nước và hyđrô trước đó đã không được quan tâm đến.
Các nhà nghiên cứu đã phát hiện ra rằng việc tăng cường sự liên kết của một loại thuốc với mục tiêu của nó, cả hai vế của liên kết hyđrô, thuốc và mục tiêu cần phải có một trong hai khả năng liên kết hydro mạnh hơn đáng kể hoặc yếu hơn đáng kể. Mặt khác, sự kết hợp liên kết hyđrô mạnh - yếu hỗn tạp suy giảm sự liên kết toàn bộ của thuốc với mục tiêu của nó, ở một số trường hợp là khoảng 3 triệu lần.
Có được những kiến thức này trong tay, các nhà nghiên cứu tiếp tục tạo ra các biến đổi hóa học trong chất ức chế InsP6 để cải thiện khả năng liên kết hyđro với các độc tố của vi khuẩn C. difficile. Một trong những sửa đổi, thay đổi một đơn nguyên tử trong InsP6, sẽ thúc đẩy liên kết InsP6 với các chất điều chế dị lập thể mạnh lên khoảng 26 lần. Quán sát này được xây dựng trên một báo cáo được công bố trên Science vào năm ngoái bởi Savidge. Các khái niệm mới này đang được triển khai nghiên cứu để có thể thiết kế chính xác các liệu phấp điều trị trong tương lai.
Nguồn: vista.gov.vn (Theo Phys.Org)
- Đột phá trong nghiên cứu RNA mở ra triển vọng điều trị các rối loạn thần kinh – cơ (07/05/2026)
- Trẻ điều trị ung thư: Suy giảm thính lực liên quan đến giảm khả năng nhận thức (22/04/2026)
- Ăn yến mạch giúp giảm cholesterol (16/04/2026)
- Các “vi sinh vật vô hình” giúp duy trì sức khỏe của chúng ta (09/04/2026)
- Dùng Tylenol khi mang thai không làm tăng nguy cơ tự kỷ, ADHD (04/04/2026)
- Làm rõ tín hiệu sinh học kích hoạt rặn trong quá trình sinh nở (25/03/2026)












